L’accident vasculaire cérébral (AVC) peut survenir à tout âge et endommager le cerveau, engendrant des séquelles parfois irréversibles. Elles font de l’AVC la première cause de handicap acquis de l’adulte. Pour améliorer l’efficacité et l’acceptabilité des parcours de prise en charge, de nouvelles méthodes reposant sur des innovations technologiques émergent.
Au travers de cette exposition, vous pourrez en apprendre plus sur l'AVC et ses répercussions, mais aussi découvrir l’une de ces approches technologiques, le neurofeedback, et comprendre son apport dans la rééducation motrice après l’AVC.
Le neur feedback en action
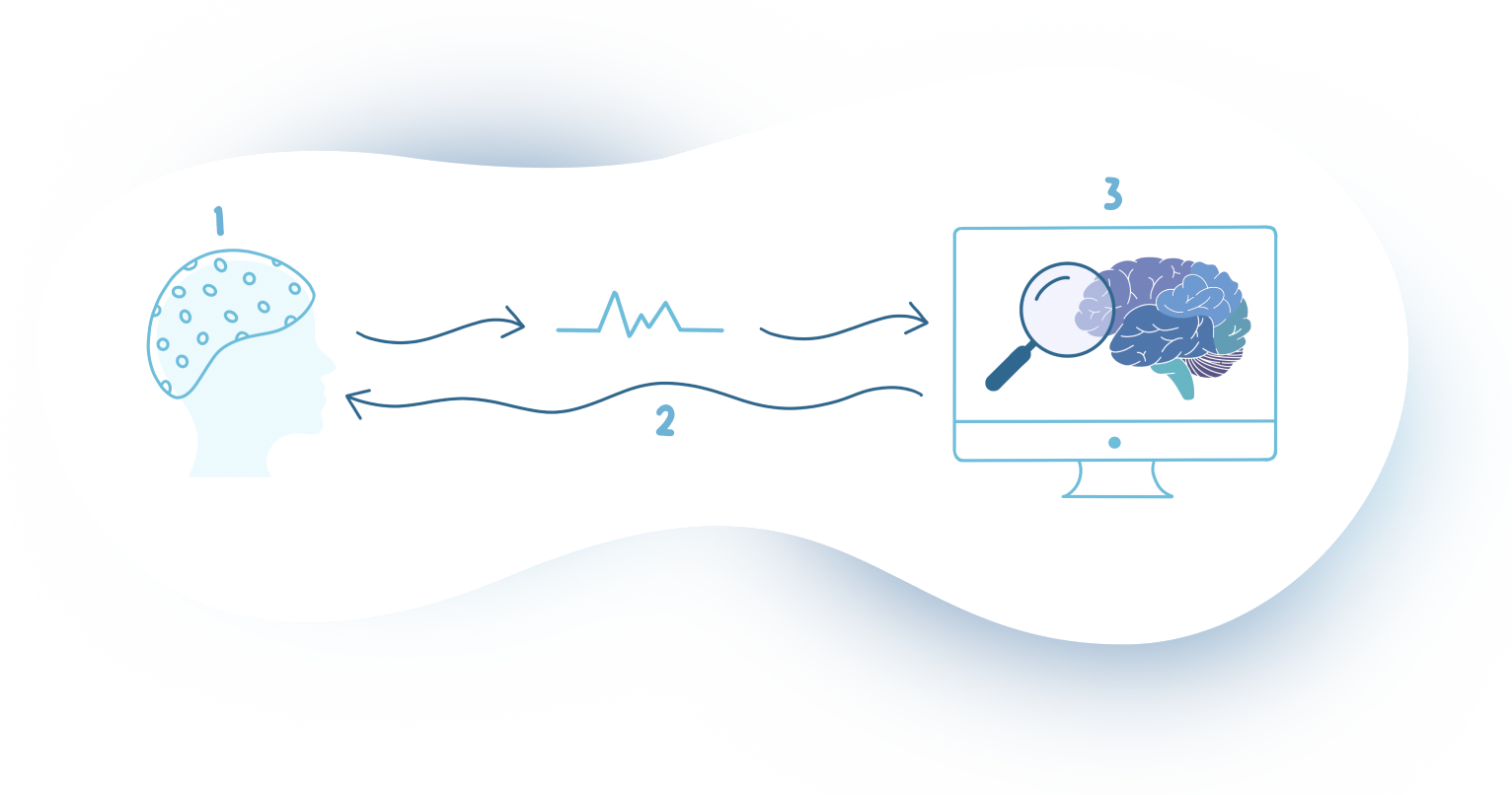
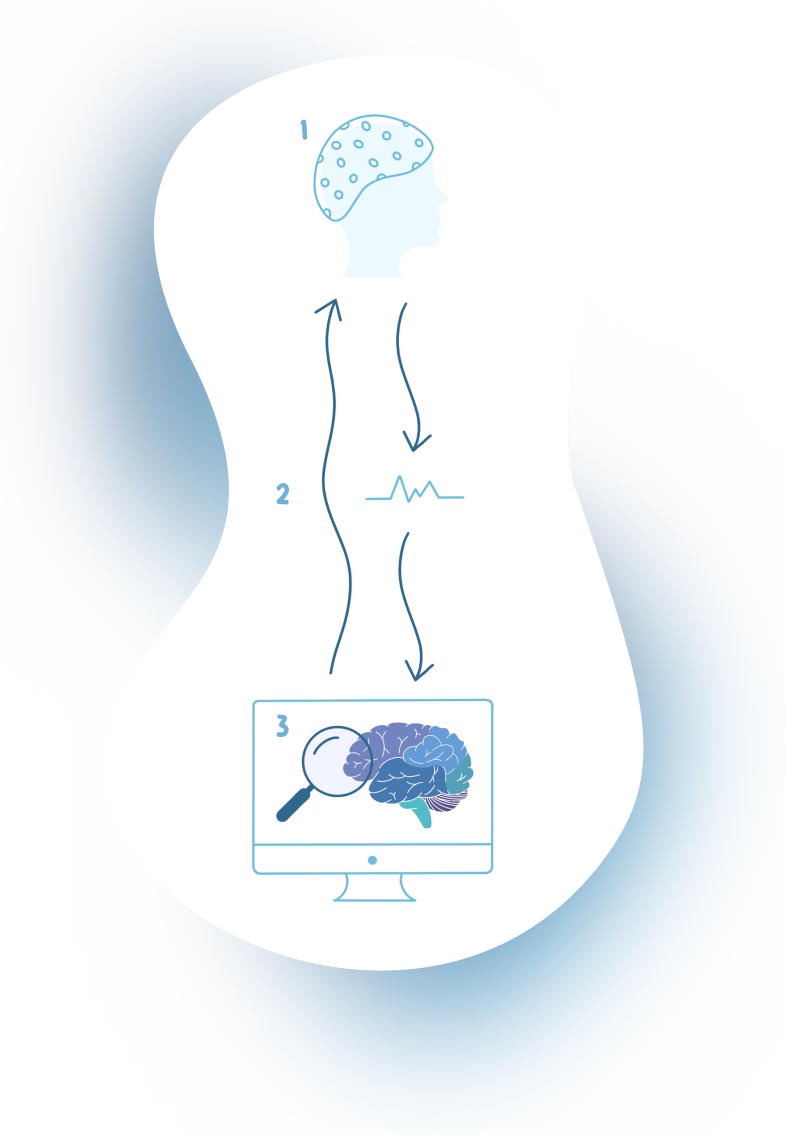
Grâce à un casque à électrodes, le dispositif de neurofeedback permet d’analyser l’activité cérébrale et de fournir un retour sensoriel en fonction de cette activité. Apprenez-en plus sur les différents éléments qui composent le système, représenté ci-dessous.
1. Les casques EEG
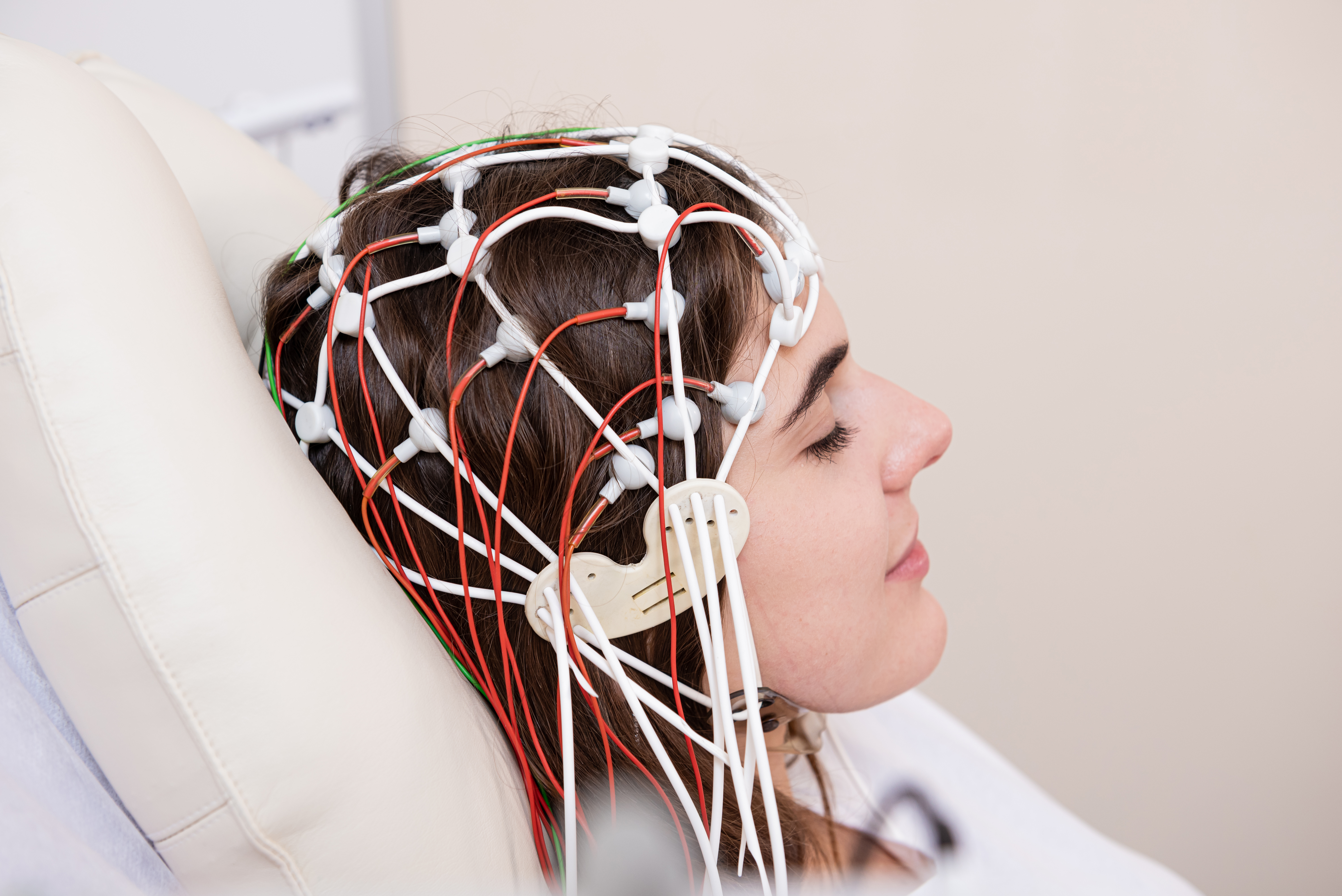
Au début du XXème siècle, Hans Berger est le premier à enregistrer l’activité cérébrale chez l’humain. Les dispositifs qu’il utilise sont cependant très simples. Par la suite, les systèmes se sont complexifiés et perfectionnés, passant de deux à plus d’une centaine d’électrodes, regroupées dans des bonnets qui rendent plus rapide leur installation.
Aujourd’hui, des systèmes de plus en plus simples d’utilisation se développent. Comportant souvent un nombre réduit de capteurs, ils permettent une installation plus rapide grâce à leurs électrodes “sèches”, qui n’ont pas besoin d’application de gel conducteur au niveau de chaque capteur, ou leurs systèmes de connectivité bluetooth. Malgré tout, ces systèmes peuvent ne pas convenir à tous les usages : il faut choisir le plus adapté à l’objectif recherché.

Années 1920

Années 1980

Années 2000

Années 2020
2. Le Feedback sensoriel
De la même manière qu'une montre connectée peut faire des retours sur le rythme cardiaque ou la respiration (biofeedback), le neurofeedback consiste à faire des retours sensoriels en fonction de l'activité du cerveau détectée par le casque EEG.
Ces retours peuvent stimuler différents sens :- le toucher : sensations tactiles générées sur le corps par des dispositifs vibrants
- l’ouïe : envoi de signaux sonores
- la vue : affichage sur un écran d’un bras virtuel qui bouge quand on imagine le mouvement
- la proprioception : mobilisation d’un membre grâce à un système robotique
Le neurofeedback permet à l’utilisateur ou à l’utilisatrice de prendre conscience de son activité mentale et donc de l’ajuster (par exemple en modifiant la manière dont il ou elle s’imagine bouger) afin de moduler au mieux les activités cérébrales ciblées et obtenir le déclenchement du retour sensoriel.
3. Capacités et limites de l'EEG
Les électrodes des casques EEG ne peuvent pas capter l’activité d’un neurone seul. Ce que l’on perçoit, c’est l’activité moyenne d’un ensemble de neurones sur une zone. Par exemple, une activation au niveau du cortex sensorimoteur est le signe que le patient est en train d'imaginer un mouvement ou de bouger son corps.
Les casques EEG permettent d’obtenir des électroencéphalogrammes comme celui-ci :

Chaque ligne correspond à l’activité d’un ensemble de neurones enregistrée par une électrode. Il n’est pas possible d’analyser directement et précisément ce signal en observant les tracés. Dans le cas du neurofeedback, ce sont des algorithmes qui permettent d’analyser et de repérer sur l’électroencéphalogramme l’activité cérébrale ciblée pour déclencher le retour sensoriel.
Qu’en pensent
les utilisateurs ?
En collaboration avec les CHU de Toulouse, Bordeaux et Montauban, l'équipe du projet ABCIS* utilise le neurofeedback pour permettre de faciliter la récupération motrice des patientes et des patients. Des patients et des soignants livrent ici le témoignage de leur expérience avec les ICO.
Qu’en dit la recherche ?
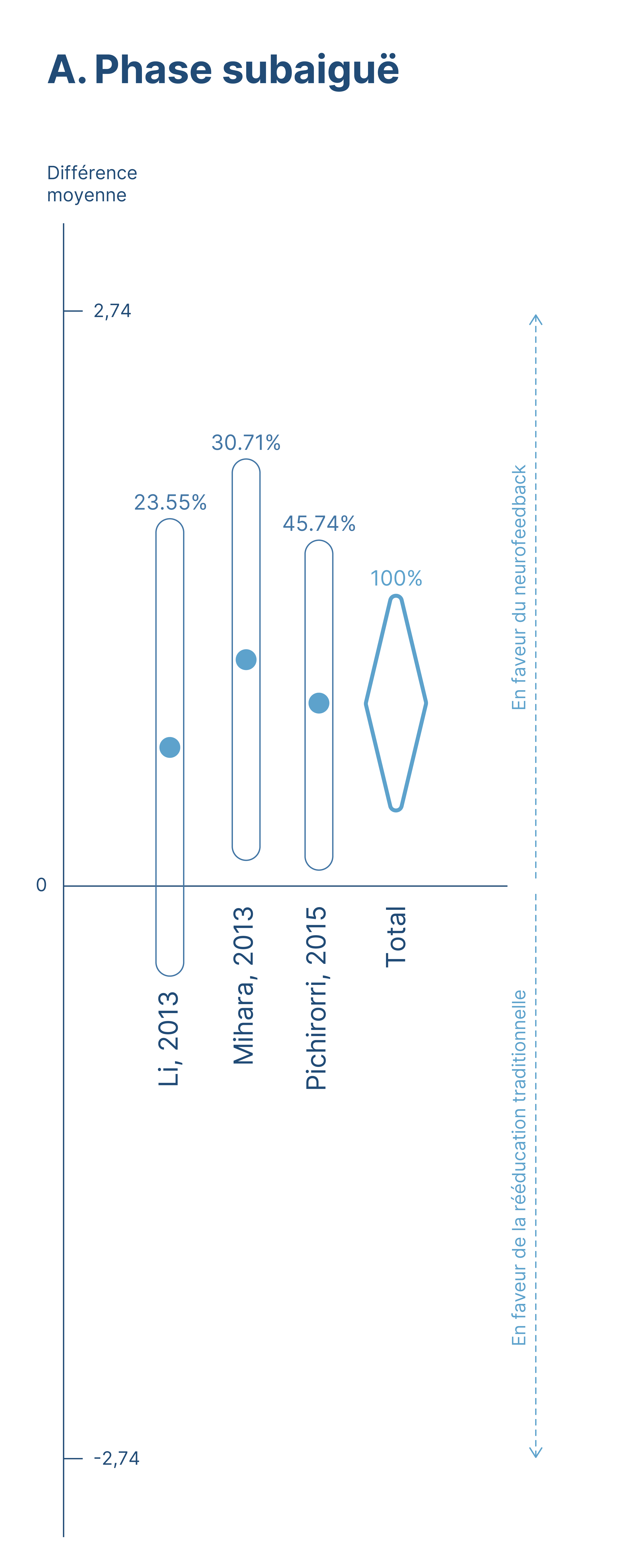
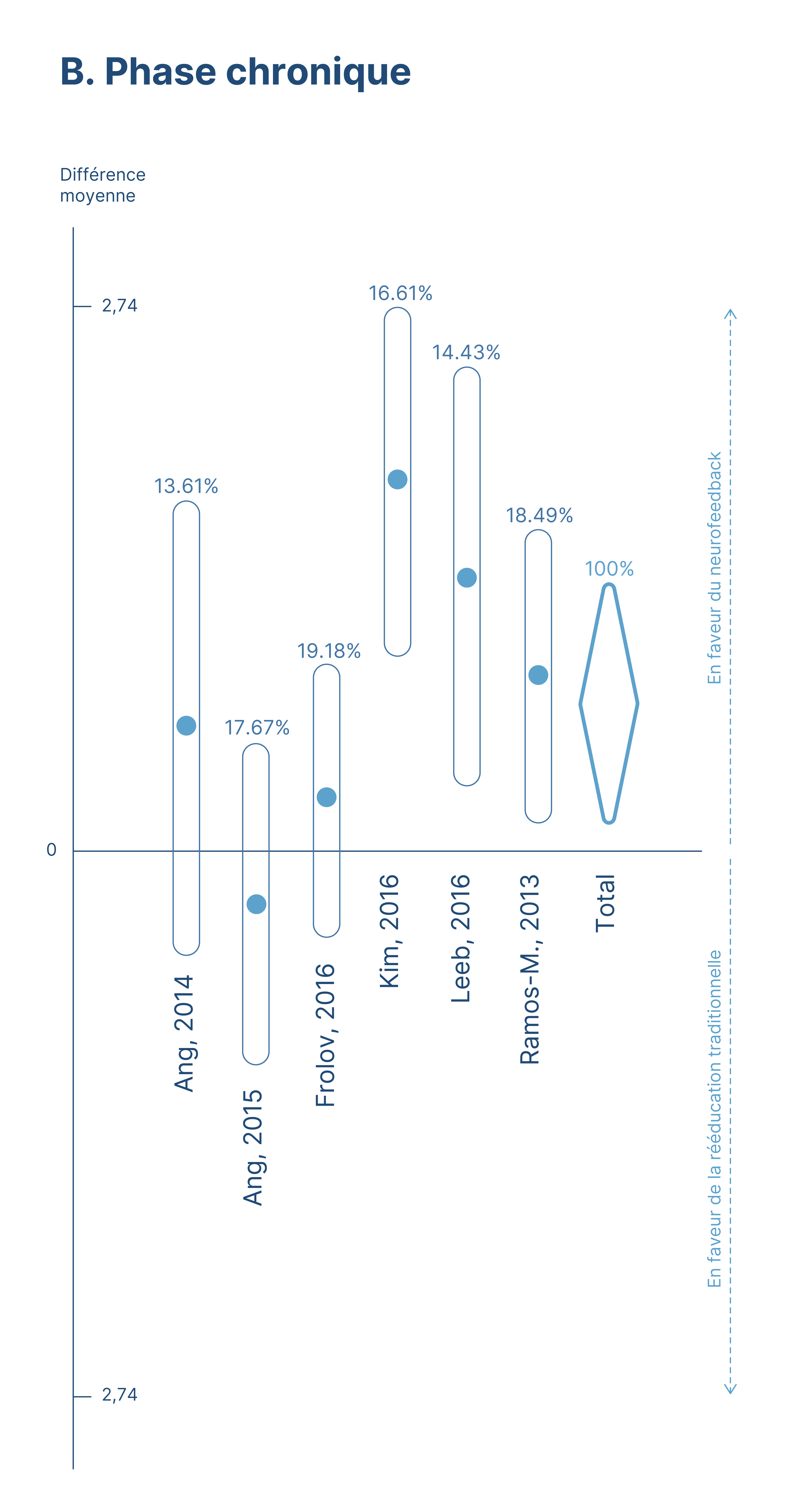
De nombreux scientifiques ont étudié cliniquement l'efficacité des ICO dans la rééducation motrice après un AVC. Ci-dessous, il s’agit d’une méta-analyse, qui inventorie et synthétise les résultats de 9 de ces études. La figure suivante est extraite de la méta-analyse.*
Dans chaque étude, il y a deux groupes de patients : un groupe expérimental qui utilise la rééducation par les ICO et un groupe contrôle qui utilise une autre technique de rééducation (par exemple une rééducation manuelle classique, ou une rééducation avec un robot).
Le graphique ci-dessus montre la différence en termes de récupération motrice entre le groupe contrôle et le groupe expérimental pour chaque étude. Si la valeur est proche de 0 alors il y a une faible différence entre les deux méthodes de rééducation. Si la valeur est positive alors la méthode est ICO a mieux fonctionné que la méthode du groupe contrôle. Dans 8 des 9 études, l’utilisation des ICO a permis d’obtenir une meilleure récupération motrice .
Le graphique A montre les effets sur la phase subaiguë (14 jours à 6 mois post AVC) tandis que le graphique B montre les effets sur la phase chronique (plus de 6 mois après l’AVC). On peut observer que pour ces deux phases, les ICO ont eu un effet plus important sur la récupération motrice que les autres techniques utilisées.
D’autres technologies peuvent entrer en jeu dans les parcours de rééducation motrice après un AVC. C’est le cas de la stimulation électrique fonctionnelle (SEF), de la réalité virtuelle (RV) et de la rééducation robotisée. Ces outils peuvent être utilisés seuls ou s’intégrer aux procédures de neurofeedback, où ils prendront le rôle du retour sensoriel.
Simulation électrique fonctionnelle (SEF)
Cette technique utilise des impulsions électriques pour activer les nerfs et les muscles, favorisant la contraction musculaire et donc l’amélioration du contrôle moteur. Dans la rééducation après un AVC, elle aide à restaurer certaines fonctions motrices, comme la marche ou la préhension.
- Effets sur la récupération motrice : Appliquée seule ou en combinaison avec d’autres thérapies (kinésithérapeute et médecins rééducateurs), la SEF s’est révélée être une approche efficace par rapport aux traitements conventionnels.
- Neuroplasticité : Pour les entraînements actifs, cela stimule la connexion cerveau-muscle, mais agit moins directement sur la plasticité cérébrale. En effet, cela ne permet pas de clore la boucle sensori-motrice, il n'y pas de synchronisation parfaite entre la commande au niveau du cerveau et la stimulation. Pour les entraînements passifs (i.e., uniquement des stimulations musculaires), le cerveau n'est pas impliqué, donc il n'y a pas de travail sur la neuroplasticité.
- Complexité d’utilisation : Demande parfois une formation spécifique, mais certains outils sont utilisables sans thérapeute.
- Coût : Variable selon l’équipement utilisé, entre 200€ à 5000€ environ.
- Accessibilité : Un certain nombre de services de rééducation physique ou de kinésithérapeutes indépendants disposent de ce type de technologies.
- Engagement du patient : Pour les entraînements passifs, le patient n'a pas de tâche à réaliser en particulier. Pour ceux actifs, il faut en général qu'il essaie de bouger en même temps.
- Effets secondaires : Irritations cutanées et sensations inconfortables possibles.
- Fatigue du patient : Fatigue musculaire possible après les séances, mais généralement bien tolérée.
Réalité virtuelle (RV)
Des exercices de rééducation sont proposés, avec soit une immersion dans un environnement virtuel interactif (avec casque de RV ou dans une salle immersive), soit sans immersion, directement sur un écran (par exemple avec une console de jeu).
- Effets sur la récupération motrice : Les systèmes de RV immersive semblent plus efficaces pour améliorer les fonctions motrices des membres supérieurs que la RV non-immersive. Plusieurs études ont montré des améliorations significatives par rapport à la thérapie conventionnelle. L'efficacité est particulièrement visible sur la qualité des mouvements, l’engagement et la motivation. Néanmoins, les études existantes sont sur de petits échantillons et peu standardisées.
- Neuroplasticité : Peut permettre de renforcer la plasticité grâce à l’apprentissage moteur et l’engagement cognitif.
- Complexité d’utilisation : Exige une familiarisation avec le matériel et les logiciels.
- Coût : Les coûts sont variables en fonction du dispositif (de plusieurs centaines à plusieurs milliers d’euros) mais évoluent très rapidement avec leur démocratisation.
- Accessibilité : Disponible dans certains centres spécialisés, encore limité.
- Engagement du patient : Forte immersion, favorise un haut niveau d’engagement.
- Effets secondaires : Pas d’effets secondaires signalés, sauf inconfort visuel possible et "cybersickness" (sensation de nausée ressentie par certaines personnes exposées à un environnement virtuel).
- Fatigue du patient : Fatigue mentale possible, notamment après une session immersive.
Rééducation robotisée (Exosquelettes)
La rééducation robotisée correspond à toutes les formes d’assistance robotisée pour guider les mouvements du patient. Les thérapeutes soulignent souvent que pour eux les robots sont un outil très utile car le nombre de répétitions permises et leur intensité sont plus importantes que ce qu'ils sont capables de faire manuellement.
- Effets sur la récupération motrice : Semble améliorer significativement la récupération motrice des patients, toutefois, ces progrès restent en deçà du seuil cliniquement significatif. L'hétérogénéité des études limite la généralisation des résultats, et davantage de protocoles sont encore nécessaires pour mieux évaluer l'efficacité et mieux comprendre ce qui la détermine (type de robot, type de tâche, type de feedback, etc).
- Neuroplasticité : L'approche robotisée permet de recréer une boucle sensorimotrice : le patient essaye de bouger, en retour le mouvement du robot permet de générer un feedback (sensoriel ou proprioceptif), et donc de clore la boucle. L'hétérogénéité des résultats en termes de récupération motrice est potentiellement liée au fait que certains protocoles ne permettent pas de clore correctement cette boucle (par exemple, si mouvement du robot n'est pas bien fait).
- Complexité d’utilisation : Différent niveau de complexité, de très complexe (comme l'exosquelette, qui nécessite un équipement lourd et une formation avancée) à plus simple, que le patient peut utiliser de manière autonome une fois installé.
- Coût : Selon les systèmes robotisés, cela peut être extrêmement coûteux (de 63 000€ à 200 000 €).
- Accessibilité : Très limitée (nécessite des centres spécialisés équipés).
- Engagement du patient : Engagement fort grâce à l’interaction avec le robot.
- Effets secondaires : Possibles douleurs musculaires ou fatigue due à l’assistance robotisée.
- Fatigue du patient : Fatigue physique importante due à la répétition des mouvements.
Guide pratique du neur feedback
Mettre en place un protocole faisant appel au neurofeedback nécessite du matériel mais aussi un encadrement particulier. À vous de trouver dans l’image les différents éléments qui composent le protocole pour en apprendre plus sur eux.
Les casques les plus efficaces à ce jour sont les casques à électrodes dites “actives”. Ils fonctionnent grâce à un gel conducteur et réduisent les artéfacts et le bruit parasites dans l’EEG (par exemple, les clignements des yeux). Ces casques sont cependant plus onéreux que les casques à électrodes dites “passives” qui peuvent être utilisés malgré leur précision plus faible, mais souvent suffisante pour les protocoles de neurofeedback. Il faut aussi disposer de casques de tailles différentes, car le bon ajustement à la tête du patient est important. À l'heure actuelle, les protocoles de neurofeedback sont souvent réalisés avec des bonnets de 32 ou 64 électrodes.
Le coût de mise en place d’un protocole de neurofeedback peut fortement varier selon le matériel utilisé. Le prix des casques, par exemple, s’étend de quelques centaines à plusieurs dizaines de milliers d’euros. Toutefois, les avancées rapides contribuent à une baisse des prix. Par ailleurs, certains services disposent déjà du matériel de base requis.
Il est recommandé de disposer d’une salle d'au moins 5 m², calme et isolée pour favoriser la concentration, où il est possible de moduler l’intensité lumineuse. Les performances des patients sont en effet souvent meilleures lorsque l’intensité lumineuse est faible, ce qui peut s’expliquer par une diminution des distractions visuelles.
Il est préférable que les séances de rééducation soient réalisées à chaque fois par la même équipe soignante (ou personne) pour garantir la cohérence et la familiarité tout au long du protocole.
L’usage des ICO n’est pas adapté à tous les profils après un AVC. En effet, certaines séquelles courantes peuvent affecter négativement les résultats de la rééducation. Par exemple, les troubles anxieux-dépressifs sont souvent associés à des troubles de l’attention; les troubles physiques à des difficultés de compréhension des consignes. Il est essentiel de créer un cadre d’écoute active pour répondre au mieux aux besoins spécifiques des patients.
L’ordinateur employé pour les sessions d’entraînement doit disposer d’un processeur 8 cœurs (Octa-Core) d’au moins 16 Go de RAM de manière à être suffisamment performant pour pouvoir traiter les données cérébrales en temps réel. La plupart des ordinateurs récents répondent à ce critère.
Par la stimulation magnétique transcrânienne de zones ciblées, on peut observer directement la qualité des connexions rétablies, particulièrement entre les zones motrices du cerveau et les membres qu’elles dirigent. En complément, iI est important d’effectuer des mesures cliniques pour évaluer la récupération motrice des patients. Des échelles existent pour quantifier les progrès en termes de mobilité des membres, comme l’échelle Fugl-Meyer (FMA-UE) ou le test Action Research Arm Test (ARAT) pour les membres supérieurs.
Le logiciel utilisé permet de lancer la séance, de calibrer les appareils, de contrôler l'acquisition des signaux EEG, de les analyser et d’envoyer des retours sensoriels en temps réel. Ces logiciels sont souvent programmés en MATLAB, C# ou Python. Medusa ou OpenVibe sont deux exemples de logiciels libres utilisés pour des sessions de rééducation grâce aux ICO. Dans le cadre du projet ABCIS, nous avons développé un logiciel “clé en main”, permettant aux cliniciens de réaliser facilement des séances de neurofeedback, sans avoir besoin de coder ou de réaliser des manipulations complexes.
Bien que les retours visuels et auditifs soient les plus fréquemment utilisés, d’autres retours sensoriels sont possibles. On peut par exemple penser aux dispositifs robotiques qui vont faire bouger le patient en simulant le mouvement naturel. D’autres systèmes comme la stimulation électrique neuromusculaire (NMES) permettent de provoquer une contraction du muscle par la stimulation électrique de nerfs moteurs.
Nécessaire pour les protocoles impliquant des retours sensoriels sonores.
Une taille d’au moins 20 pouces est recommandée pour afficher les retours sensoriels visuels.
Cet outil permet d’enregistrer en temps réel les données. Pour cela, il est nécessaire d’avoir un amplificateur EEG avec une résolution minimale de 16 bits, un taux d'échantillonnage d'au moins 256 Hz, et une capacité de communication câblée ou sans fil avec un ordinateur. Les systèmes EEG médicaux utilisés en clinique répondent à ces critères.

Casque EEG
Les casques les plus efficaces à ce jour sont les casques à électrodes dites “actives”. Ils fonctionnent grâce à un gel conducteur et réduisent les artéfacts et le bruit parasites dans l’EEG (par exemple, les clignements des yeux). Ces casques sont cependant plus onéreux que les casques à électrodes dites “passives” qui peuvent être utilisés malgré leur précision plus faible, mais souvent suffisante pour les protocoles de neurofeedback. Il faut aussi disposer de casques de tailles différentes, car le bon ajustement à la tête du patient est important. À l'heure actuelle, les protocoles de neurofeedback sont souvent réalisés avec des bonnets de 32 ou 64 électrodes.
Le budget
Le coût de mise en place d’un protocole de neurofeedback peut fortement varier selon le matériel utilisé. Le prix des casques, par exemple, s’étend de quelques centaines à plusieurs dizaines de milliers d’euros. Toutefois, les avancées rapides contribuent à une baisse des prix. Par ailleurs, certains services disposent déjà du matériel de base requis.
Une salle dédiée
Il est recommandé de disposer d’une salle d'au moins 5 m², calme et isolée pour favoriser la concentration, où il est possible de moduler l’intensité lumineuse. Les performances des patients sont en effet souvent meilleures lorsque l’intensité lumineuse est faible, ce qui peut s’expliquer par une diminution des distractions visuelles.
Le personnel soignant
Il est préférable que les séances de rééducation soient réalisées à chaque fois par la même équipe soignante (ou personne) pour garantir la cohérence et la familiarité tout au long du protocole.
Le patient
L’usage des ICO n’est pas adapté à tous les profils après un AVC. En effet, certaines séquelles courantes peuvent affecter négativement les résultats de la rééducation. Par exemple, les troubles anxieux-dépressifs sont souvent associés à des troubles de l’attention; les troubles physiques à des difficultés de compréhension des consignes. Il est essentiel de créer un cadre d’écoute active pour répondre au mieux aux besoins spécifiques des patients.
Ordinateur
L’ordinateur employé pour les sessions d’entraînement doit disposer d’un processeur 8 cœurs (Octa-Core) d’au moins 16 Go de RAM de manière à être suffisamment performant pour pouvoir traiter les données cérébrales en temps réel. La plupart des ordinateurs récents répondent à ce critère.
Mesures complémentaires
Par la stimulation magnétique transcrânienne de zones ciblées, on peut observer directement la qualité des connexions rétablies, particulièrement entre les zones motrices du cerveau et les membres qu’elles dirigent. En complément, iI est important d’effectuer des mesures cliniques pour évaluer la récupération motrice des patients. Des échelles existent pour quantifier les progrès en termes de mobilité des membres, comme l’échelle Fugl-Meyer (FMA-UE) ou le test Action Research Arm Test (ARAT) pour les membres supérieurs.
Logiciel
Le logiciel utilisé permet de lancer la séance, de calibrer les appareils, de contrôler l'acquisition des signaux EEG, de les analyser et d’envoyer des retours sensoriels en temps réel. Ces logiciels sont souvent programmés en MATLAB, C# ou Python. Medusa ou OpenVibe sont deux exemples de logiciels libres utilisés pour des sessions de rééducation grâce aux ICO. Dans le cadre du projet ABCIS, nous avons développé un logiciel “clé en main”, permettant aux cliniciens de réaliser facilement des séances de neurofeedback, sans avoir besoin de coder ou de réaliser des manipulations complexes.
Retours sensoriels
Bien que les retours visuels et auditifs soient les plus fréquemment utilisés, d’autres retours sensoriels sont possibles. On peut par exemple penser aux dispositifs robotiques qui vont faire bouger le patient en simulant le mouvement naturel. D’autres systèmes comme la stimulation électrique neuromusculaire (NMES) permettent de provoquer une contraction du muscle par la stimulation électrique de nerfs moteurs.
Haut-parleur
Nécessaire pour les protocoles impliquant des retours sensoriels sonores.
Écran d'ordinateur
Une taille d’au moins 20 pouces est recommandée pour afficher les retours sensoriels visuels.
Amplificateur de signaux EEG
Cet outil permet d’enregistrer en temps réel les données. Pour cela, il est nécessaire d’avoir un amplificateur EEG avec une résolution minimale de 16 bits, un taux d'échantillonnage d'au moins 256 Hz, et une capacité de communication câblée ou sans fil avec un ordinateur. Les systèmes EEG médicaux utilisés en clinique répondent à ces critères.
Vous souhaitez en apprendre plus sur les différents sujets abordés dans cette exposition ? Les compléments suivants ont été rassemblés pour vous permettre de prolonger vos découvertes. Vous pourrez également retrouver du contenu additionnel dans la partie “ressources” de cette exposition.
Carte interactive
Cette carte intéractive répertorie les associations locales qui peuvent accompagner les patients, les patientes et leurs proches après un AVC, mais aussi les structures qui participent à la recherche sur le neurofeedback en santé.
Cliquez pour découvrir les différents centres de recherche, services hospitaliers ou associations dans votre région !
Vous s
uhaitez
en savoir plus ?
Voici une sélection de ressources organisées par thématique : des informations générales sur l’AVC, de la littérature scientifique sur le neurofeedback, ainsi que des informations complémentaires sur les interfaces cerveau-ordinateur.